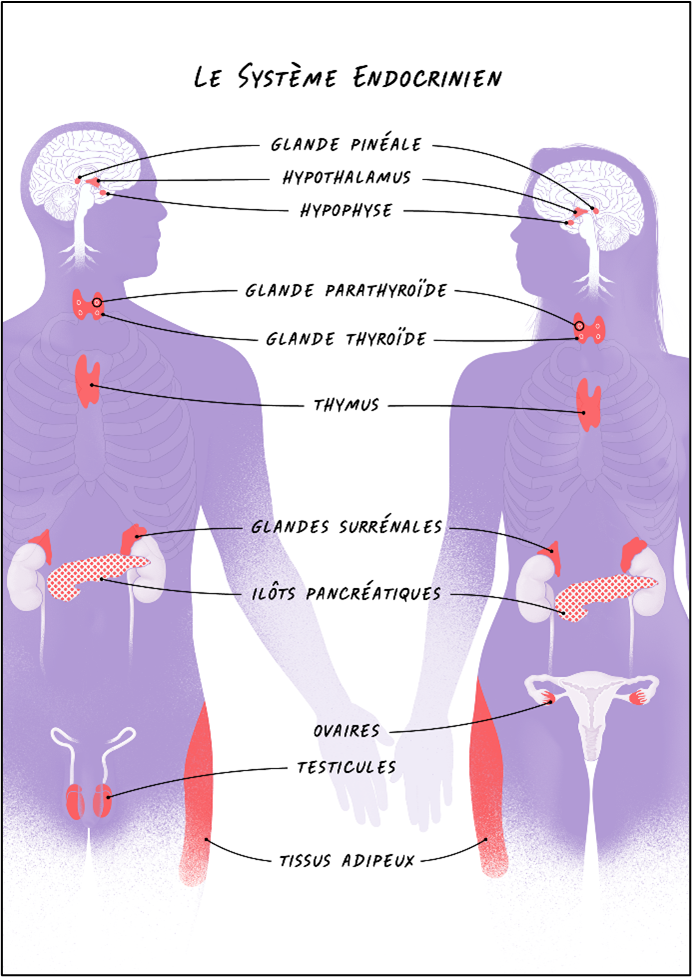
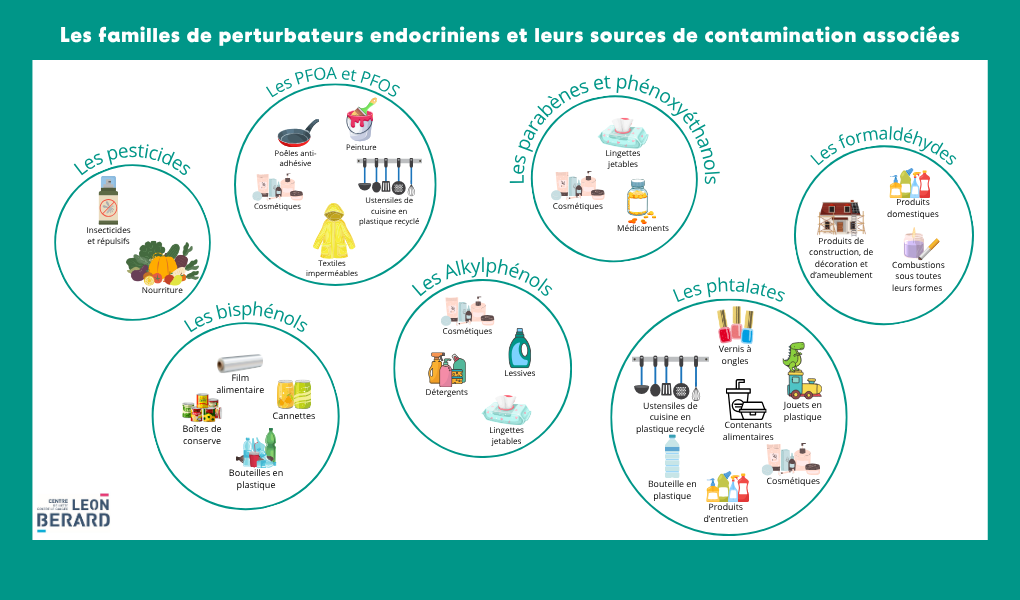
Les effets des PE sur la santé humaine sont encore en discussion à ce jour. Néanmoins, un certain nombre d’affections sont aujourd’hui suspectées d’être la conséquence d’exposition aux PE sur :
- Le système reproducteur masculin : cryptorchidie, malformations, baisse de la testostérone, puberté précoce
- Le système reproducteur féminin : augmentation de la fréquence d’anomalies du développement du tractus génital, endométriose, puberté précoce
- L’augmentation de diverses anomalies : pathologies métaboliques, obésité, diabète insulinodépendant, prématurité, troubles du système nerveux, hyperactivité…
Enfin, le rôle des PE est aussi suspecté pour les cancers dont le développement est influencé par des mécanismes hormonaux, autrement dit, les cancers hormono-dépendants (Gore, 2015).
En population générale
Certaines substances PE sont connues pour leurs effets avérés ou suspectés dans l’apparition de cancers hormono-dépendants (sein, utérus, prostate, testicule). Parmi ceux-ci, on peut lister :
Chlordécone
Insecticide organochloré utilisé dans les Antilles jusqu’aux années 1990, il est persistant dans l’environnement et bioaccumulable (eaux, sols, aliments d’origine végétale ou animale). Il est classé peut-être cancérogène pour l’humain (Groupe 2B) par le CIRC. De récentes études montrent une relation entre exposition au chlordécone et la survenue du cancer de la prostate (Anses, 2024), mais le lien de causalité reste encore à établir. Un état des lieux du cancer de la prostate aux Antilles françaises a révélé une incidence et mortalité plus élevées qu’en France métropolitaine mais en accord avec les origines africaines de la majorité de la population. D’autres études devront approfondir l’identification des déterminants des facteurs de risque de survenue et d’agressivité au diagnostic du cancer mais également les déterminants de son évolution clinique (Multigner, 2016). Les cancers de la prostate provoqués par les pesticides, dont le chlordécone, sont reconnus comme maladie professionnelle depuis le 22 décembre 2021 (Gouvernement.fr, 2021).
Contraceptifs oraux estroprogestatifs
Ils sont associés à une augmentation du risque de cancer du sein et du cancer du col de l’utérus. Les risques seraient associés à une prise de contraception orale pendant plus de 8 ans. Il est important de noter que la pilule à base de progestatifs uniquement ne semble pas concernée par ce risque de cancer (Inca, 2023).
Diéthylstilbestrol (Distilbène® ou DES)
Prescrit dans les années 1950-1960 pour prévenir des arrêts spontanés de grossesse, il a été interdit en France en 1977. Des études ont mis en évidence un lien entre l’administration de diéthylstilbestrol à des femmes enceintes et la survenue de cancers du vagin, du sein (Palmer, 2006), du col et de l’utérus chez les filles des mères traitées (Réseau DES France, 2010) mais également des malformations génitales ou des conséquences sur leur fertilité (JO du Sénat, 1992).
Dioxines
La dioxine de Seveso (2,3,7,8 TCDD, nommée ainsi suite à l’explosion de l’usine de pesticides ICMESA de Seveso en Italie) est classée cancérogène certain (Groupe 1) pour l’humain par le CIRC. Une relation significative a été mise en évidence entre l’exposition aux anciens incinérateurs d’ordures ménagères et le risque de cancer : on observe une augmentation de la fréquence globale de cancers chez la femme (= tous types de cancers), et en particulier de cancer du sein et les lymphomes malins non hodgkiniens ; les résultats montrent également un excès de risque de myélome multiple chez les hommes (BEH, 2009). Il convient cependant de rappeler que l’exposition à de fortes doses de la dioxine de Seveso représente une situation exceptionnelle puisqu’elle résulte d’un accident. Depuis 2005, les incinérateurs sont soumis à une directive qui prévoit des mesures strictes pour traiter leurs fumées. Des études récentes ont également exploré un lien potentiel avec le cancer de la thyroïde, sans conclusion définitive. Il s’agit d’un facteur de risque suspecté qui confirme la nécessité de réaliser de futures études sur l’humain dont l’exposition aux dioxines dans l’environnement est persistante (Van Gerwen, 2023).
Une étude sur l’exposition environnementale aux dioxines a fait l’objet de deux sujets de thèse au sein du Département Prévention, Cancer, Environnement du Centre Léon Bérard.
- La première thèse en expologie environnementale a permis l’inventaire des sources émettrice de dioxines en France et la création d’une métrique d’exposition aux dioxines pour les études épidémiologiques (Coudon, 2019).
- La seconde thèse en épidémiologie a porté sur l’exposition alimentaire (première source d’exposition) et atmosphérique aux dioxines. Ainsi, l’impact de l’exposition aux dioxines, par l’alimentation, sur le risque de cancer du sein a été évaluée au sein de la cohorte E3N-Générations. La cohorte E3N-Générations est une Etude Epidémiologique auprès de femmes de la MGEN (Mutuelle Générale de l’Education Nationale). Il s’agit d’une enquête de cohorte prospective portant sur environ 100 000 femmes volontaires françaises nées entre 1925 et 1950 et suivies depuis 1990. Cette étude s’intéresse aux relations entre l’apparition des cancers et les caractéristiques individuelles et environnementales des femmes de l’étude. Aucune association n’a été observée, à l’exception d’une diminution du risque de cancer du sein hormono-indépendant, retrouvée de façon significative dans l’étude alimentaire. Cette dernière observation est cohérente avec des données expérimentales. L’exposition atmosphérique aux dioxines a ensuite été étudiée dans le cadre du projet XENAIR. Les résultats des analyses suggèrent une augmentation du risque de cancer du sein associée avec une augmentation de l’exposition aux dioxines (Praud, 2024).
Formaldéhyde
Le formaldéhyde est un cancérogène avéré, impliqué dans le développement de la leucémie et de cancer du nasopharynx.
HAP (hydrocarbures aromatiques polycycliques)
Groupe de plus de 100 composés organiques produits lors de la combustion incomplète ou de la pyrolyse de matières organiques. Certains HAP sont classés comme cancérogènes par le CIRC et sont suspectés de pouvoir être liés aux développements de cancers de la peau, du poumon, de la vessie, du foie et de sein (Jubber, 2023 ; Mallah, 2022 ; Rocha, 2021).
PCB (polychlorobiphényles)
Composés organiques de synthèse interdits en France depuis 1987. L’exposition aux PCB semble liée au développement de mélanomes malins. Une association a également été constatée pour l’apparition de lymphome non Hodgkinien et de cancer du sein.
Phtalates
Plastifiants largement utilisés dans des produits de consommation courante (PVC : ballons, nappes, rideaux de douche, anneaux de dentition, colles…). Des études suggèrent un lien avec la survenue de cancers, notamment tumeurs du foie, testiculaires, de la prostate ou encore du sein. Des études plus poussées sont nécessaires pour valider ces associations (Guo, 2023 ; Anses, 2024 ; Inserm 2018 ; Liu, 2021).
En population professionnelle
Les effets des perturbateurs endocriniens chez les travailleurs exposés font l’objet d’un nombre croissant d’études. Les expositions dans les secteurs agricoles, chimiques et pharmaceutiques sont souvent plus importantes que dans la population générale.
Partant du fait que plusieurs perturbateurs endocriniens sont également des pesticides, des études se sont intéressées au lien entre exposition professionnelle aux pesticides et apparition de cancers hormonodépendants chez les agriculteurs (prostate, testicule, sein, ovaire). Bien que les résultats soient souvent divergents, certaines études tendent à montrer une plus forte incidence de cancers hormonodépendants chez les agriculteurs ou agricultrices utilisateurs de pesticides (Alavanja, 2005 ; Buranatrevedh, 2001 ; Ibarluzea, 2004). Des recherches supplémentaires sont nécessaires pour clarifier le rôle de chacune des molécules potentiellement responsables (certains organochlorés, triazine) dans l’apparition de ces cancers, cette identification n’ayant pas été effectuée lors des recherches précédentes (INRS, 2002).
- Le projet SIGEXPOSOME, mené par le Centre Léon Bérard en 2016 vise à améliorer la caractérisation de l’exposition aux pesticides en population générale et améliorer les connaissances concernant les paramètres génétiques et biologiques impliques dans la survenue de cancers. Le recrutement des participants volontaires (hommes résidants près d’une zone viticole) s’est effectué en juillet, octobre 2016 et février 2017. La méthodologie a conduit à des prélèvements sanguins et urinaires et de poussières à domicile et à l’utilisation d’un SIG.
- La cohorte AGRICAN est une étude épidémiologique de grande envergure qui suit depuis 2005 plus de 180 000 affiliés à la Mutualité Sociale Agricole (MSA). Les données collectées ont mis en évidence des associations entre l’exposition aux pesticides, dont certains sont des PE, et une augmentation du risque de certains cancers, notamment de la prostate.
En 2022, une étude s’est intéressée à l’exposition à 17 perturbateurs endocriniens dans différents milieux professionnels, à partir des données de la cohorte canadienne CanCHEC. L’exposition a été estimée selon les types d’emplois (par exemple : agriculture, industrie chimique, soins de santé, etc.), et six substances ont été associées à un risque modifié de cancer colorectal. Toutefois, la direction des associations (augmentation ou diminution du risque) variait selon les substances étudiées (Pelland-St-Pierre, 2022).