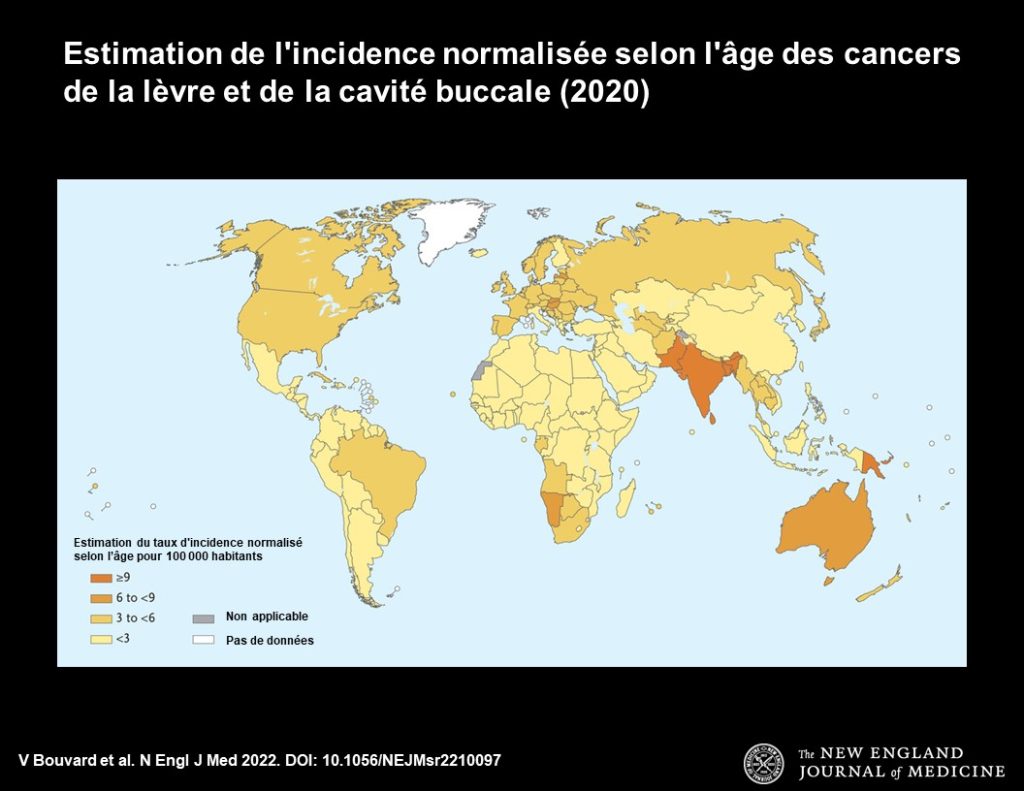
1. Global Cancer Observatory. Cancer today. Lyon, France: International Agency for Research on Cancer, 2020 (https://gco .iarc.fr/today).
2. Johnson NW, Gupta B, Speicher DJ, et al. Etiology and risk factors. In: Shah J, Johnson NW, eds. Oral and oropharyngeal cancer. 2nd ed. Boca Raton, FL: CRC Press, 2018:19-94.
3. Betel-quid and areca-nut chewing and some areca-nut derived nitrosamines: IARC monographs on the evaluation of carcinogenic risks to humans, vol. 85. Lyon, France: International Agency for Research on Cancer, 2004 (https://publications.iarc .fr/103).
4. Smokeless tobacco (SLT) products. Geneva: World Health Organization, January 10, 2018 (https://extranet.who.int/ fctcapps/fctcapps/fctc/kh/slt/news/smokeless-tobacco-slt -products).
5. de Martel C, Plummer M, Vignat J, Franceschi S. Worldwide burden of cancer attributable to HPV by site, country and HPV type. Int J Cancer 2017;141:664-70.
6. Bouvard V, Wentzensen N, Mackie A, et al. The IARC perspective on cervical cancer screening. N Engl J Med 2021;385: 1908-18.
7. IARC Handbooks of Cancer Prevention: preamble for primary prevention. Lyon, France: International Agency for Research on Cancer, October 2019 (https://handbooks.iarc.fr/ documents-handbooks/hb-preamble-primary-prevention.pdf).
8. IARC Handbooks of Cancer Prevention: preamble for secondary prevention. Lyon, France: International Agency for Research on Cancer, October 2019 (https://handbooks.iarc.fr/ documents-handbooks/hb-preamble-secondary-prevention.pdf).
9. Tobacco control: reversal of risk after quitting smoking. IARC Handbooks of Cancer Prevention. Vol. 11. Lyon, France: International Agency for Research on Cancer, 2007 (https://publications.iarc.fr/381).
10. Freedman ND, Abnet CC, Leitzmann MF, Hollenbeck AR, Schatzkin A. Prospective investigation of the cigarette smokinghead and neck cancer association by sex. Cancer 2007;110:1593- 601.
11. Maasland DH, van den Brandt PA, Kremer B, Goldbohm RAS, Schouten LJ. Alcohol consumption, cigarette smoking and the risk of subtypes of head-neck cancer: results from the Netherlands Cohort Study. BMC Cancer 2014;14:187.
12. De Stefani E, Boffetta P, Deneo-Pellegrini H, et al. The effect of smoking and drinking in oral and pharyngeal cancers: a case-control study in Uruguay. Cancer Lett 2007;246:282-9.
13. Radoï L, Paget-Bailly S, Cyr D, et al. Tobacco smoking, alcohol drinking and risk of oral cavity cancer by subsite: results of a French population-based case-control study, the ICARE study. Eur J Cancer Prev 2013;22:268-76.
14. Marron M, Boffetta P, Zhang Z-F, et al. Cessation of alcohol drinking, tobacco smoking and the reversal of head and neck cancer risk. Int J Epidemiol 2010;39:182-96.
15. Warnakulasuriya S, Kujan O, Aguirre-Urizar JM, et al. Oral potentially malignant disorders: a consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis 2021;27:1862-80.
16. Gupta PC, Murti PR, Bhonsle RB, Mehta FS, Pindborg JJ. Effect of cessation of tobacco use on the incidence of oral mucosal lesions in a 10-yr follow-up study of 12,212 users. Oral Dis 1995; 1:54-8.
17. Hashibe M, Sankaranarayanan R, Thomas G, et al. Alcohol drinking, body mass index and the risk of oral leukoplakia in an Indian population. Int J Cancer 2000;88:129-34.
18. Luo J, Ye W, Zendehdel K, et al. Oral use of Swedish moist snuff (snus) and risk for cancer of the mouth, lung, and pancreas in male construction workers: a retrospective cohort study. Lancet 2007;369:2015-20.
19. Boffetta P, Aagnes B, Weiderpass E, Andersen A. Smokeless tobacco use and risk of cancer of the pancreas and other organs. Int J Cancer 2005;114:992-5.
20. Lewin F, Norell SE, Johansson H, et al. Smoking tobacco, oral snuff, and alcohol in the etiology of squamous cell carcinoma of the head and neck: a population-based case-referent study in Sweden. Cancer 1998;82:1367-75.
21. Schildt EB, Eriksson M, Hardell L, Magnuson A. Oral snuff, smoking habits and alcohol consumption in relation to oral cancer in a Swedish case-control study. Int J Cancer 1998;77:341-6.
22. Rosenquist K. Risk factors in oral and oropharyngeal squamous cell carcinoma: a population-based case-control study in southern Sweden. Swed Dent J Suppl 2005;(179):1-66.
23. Nasher AT, Al-Hebshi NN, Al-Moayad EE, Suleiman AM. Viral infection and oral habits as risk factors for oral squamous cell carcinoma in Yemen: a case-control study. Oral Surg Oral Med Oral Pathol Oral Radiol 2014;118(6):566-572.e1.
24. Wu YH, Yen CJ, Hsiao JR, et al. A comprehensive analysis on the association between tobacco-free betel quid and risk of head and neck cancer in Taiwanese men. PLoS One 2016;11(10):e0164937.
25. Gupta R, Mariano LC, Nethan ST, et al. Risk reversal of oral, pharyngeal and oesophageal cancers after cessation of betel quid users: a systematic review and meta-analysis. Ann Glob Health 2022;88:5.
26. Gupta PC, Mehta FS, Pindborg JJ, et al. Intervention study for primary prevention of oral cancer among 36 000 Indian tobacco users. Lancet 1986;1:1235-9.
27. Hashibe M, Mathew B, Kuruvilla B, et al. Chewing tobacco, alcohol, and the risk of erythroplakia. Cancer Epidemiol Biomarkers Prev 2000;9:639-45.
28. Gupta PC, Mehta FS, Pindborg JJ, et al. Primary prevention trial of oral cancer in india: a 10-year follow-up study. J Oral Pathol Med 1992;21:433-9.
29. Anantha N, Nandakumar A, Vishwanath N, et al. Efficacy of an anti-tobacco community education program in India. Cancer Causes Control 1995;6:119-29.
30. Severson HH, Andrews JA, Lichtenstein E, Gordon JS, Barckley MF. Using the hygiene visit to deliver a tobacco cessation program: results of a randomized clinical trial. J Am Dent Assoc 1998;129:993-9.
31. Severson HH, Gordon JS, Danaher BG, Akers L. ChewFree. com: evaluation of a Web-based cessation program for smokeless tobacco users. Nicotine Tob Res 2008;10:381-91.
32. Severson HH, Peterson AL, Andrews JA, et al. Smokeless tobacco cessation in military personnel: a randomized controlled trial. Nicotine Tob Res 2009;11:730-8.
33. Walsh MM, Hilton JF, Masouredis CM, Gee L, Chesney MA, Ernster VL. Smokeless tobacco cessation intervention for college athletes: results after 1 year. Am J Public Health 1999;89:228-34.
34. Walsh MM, Langer TJ, Kavanagh N, et al. Smokeless tobacco cessation cluster randomized trial with rural high school males: intervention interaction with baseline smoking. Nicotine Tob Res 2010;12:543-50.
35. Gansky SA, Ellison JA, Rudy D, et al. Cluster-randomized controlled trial of an athletic trainer-directed spit (smokeless) tobacco intervention for collegiate baseball athletes: results after 1 year. J Athl Train 2005;40:76-87.
36. Raja M, Saha S, Krishna-Reddy V, Mohd S, Narang R, Sood P. Effectiveness of oral health education versus nicotine replacement therapy for tobacco cessation — a parallel randomized clinical trial. J Clin Exp Dent 2016;8(1):e64-e70.
37. Severson HH, Danaher BG, Ebbert JO, et al. Randomized trial of nicotine lozenges and phone counseling for smokeless tobacco cessation. Nicotine Tob Res 2015;17:309-15.
38. Hung L-C, Kung P-T, Lung C-H, et al. Assessment of the risk of oral cancer incidence in a high-risk population and establishment of a predictive model for oral cancer incidence using a population-based cohort in Taiwan. Int J Environ Res Public Health 2020;17:665.
39. Fagerström K, Gilljam H, Metcalfe M, Tonstad S, Messig M. Stopping smokeless tobacco with varenicline: randomised double blind placebo controlled trial. BMJ 2010;341:c6549.
40. Mehrotra R, Yadav A, Sinha DN, et al. Smokeless tobacco control in 180 countries across the globe: call to action for full implementation of WHO FCTC measures. Lancet Oncol 2019; 20(4):e208-e217.
41. Huang J, Chaloupka FJ. The impact of the 2009 Federal Tobacco Excise Tax increase on youth tobacco use. Cambridge, MA: National Bureau of Economic Research, April 2012 (https:// www.nber.org/papers/w18026).
42. Nargis N, Hussain AK, Fong GT. Smokeless tobacco product prices and taxation in Bangladesh: findings from the International Tobacco Control Survey. Indian J Cancer 2014;51:Suppl 1: S33-S38.
43. John RM. Price elasticity estimates for tobacco products in India. Health Policy Plan 2008;23:200-9.
44. Joseph RA, Chaloupka FJ. The influence of prices on youth tobacco use in India. Nicotine Tob Res 2014;16:Suppl 1:S24-S29.
45. Selvaraj S, Srivastava S, Karan A. Price elasticity of tobacco products among economic classes in India, 2011–2012. BMJ Open 2015;5(12):e008180.
46. Walsh T, Warnakulasuriya S, Lingen MW, et al. Clinical assessment for the detection of oral cavity cancer and potentially malignant disorders in apparently healthy adults. Cochrane Database Syst Rev 2021;12:CD010173.
47. Sankaranarayanan R, Ramadas K, Thara S, et al. Long term effect of visual screening on oral cancer incidence and mortality in a randomized trial in Kerala, India. Oral Oncol 2013;49:314-21.
48. Sankaranarayanan R, Fernandez Garrote L, Lence Anta J, Pisani P, Rodriguez Salva A. Visual inspection in oral cancer screening in Cuba: a case-control study. Oral Oncol 2002;38: 131-6.
49. Chuang S-L, Su WW-Y, Chen SL-S, et al. Population-based screening program for reducing oral cancer mortality in 2,334,299 Taiwanese cigarette smokers and/or betel quid chewers. Cancer 2017;123:1597-609.
50. Ho P-S, Wang W-C, Huang Y-T, Yang Y-H. Finding an oral potentially malignant disorder in screening program is related to early diagnosis of oral cavity cancer — experience from real world evidence. Oral Oncol 2019;89:107-14.
51. Moyer VA; U.S. Preventive Services Task Force. Screening for oral cancer: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med 2014;160:55-60.
52. Warnakulasuriya S, Kerr AR. Oral cancer screening: past, present, and future. J Dent Res 2021;100:1313-20.
53. Seventy-Fourth World Health Assembly. Oral health. Geneva: World Health Organization, May 31, 2021 (https://apps.who.int/gb/ebwha/pdf_files/WHA74/A74_R5-en.pdf).